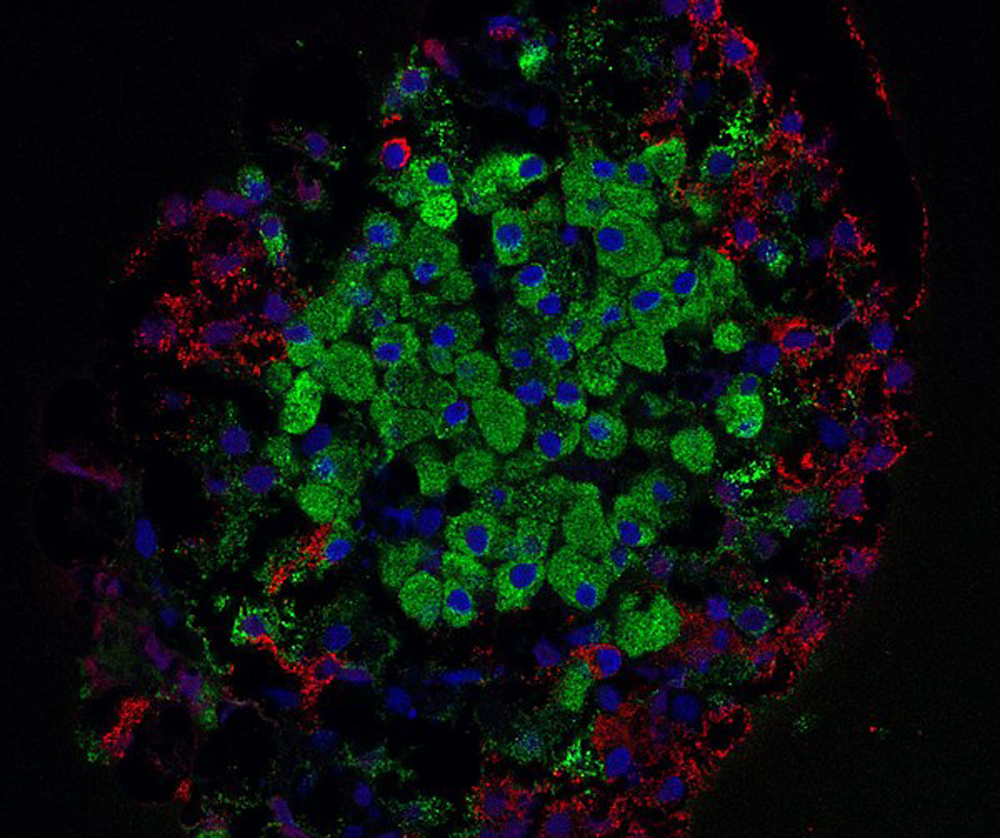
La generazione di organoidi funzionali simili a isole pancreatiche umane (human islet-like organoids – HILOs), in grado di ripristinare l’omeostasi del glucosio, sembra ormai essere possibile, almeno nei topi. È quanto dimostra un recente studio, pubblicato sulla rivista Nature, in cui gli organoidi non hanno subito alcun processo di rigetto immunitario, dopo il trapianto in topi diabetici.
Diabete e isole pancreatiche
Le isole pancreatiche, note come isole di Langerhans, sono le regioni del pancreas che contengono le sue cellule endocrine. Un gran numero di recettori accoppiati a proteine G regolano la secrezione di insulina, glucagone e somatostatina da questi gruppi di cellule. Alcune di queste proteine sono i bersagli di farmaci usati per trattare il diabete di tipo 2.
Si pensa che le cellule beta delle isole pancreatiche vengano distrutte da fenomeni autoimmunitari. Tuttavia, ci sono anche indicazioni che queste cellule siano semplicemente diventate non funzionali.
Ricercatori di tutto il mondo stanno attivamente cercando di perfezionare il trapianto di isole, come mezzo per ripristinare la funzione fisiologica delle cellule beta, ripristinando il controllo del glucosio a lungo termine nelle persone con diabete di tipo 1 e di tipo 2 in stadio avanzato. Le isole ottenute da cadaveri variano però in qualità e sono limitate nella disponibilità. Le cellule beta pancreatiche produttrici di insulina derivate da cellule staminali umane potrebbero fornire una soluzione a lungo termine nei pazienti affetti da diabete insulino-dipendente o dal trapianto. Purtroppo però la generazione di cellule beta funzionali è ancora un processo difficile.
Diabete e isole pancreatiche: la via di segnalazione Wnt
Ronald Evans e colleghi riportano una tecnica per la generazione di HILOs tridimensionali che potrebbe rappresentare una fonte alternativa di cellule endocrine trapiantabili. Queste sarebbero in grado di ripristinare il controllo glicemico a lungo termine, senza la necessità di immunosoppressione cronica.
Gli autori sfruttano la via di segnalazione Wnt per facilitare la maturazione metabolica degli HILOs necessari per la secrezione di insulina. Inoltre, il loro metodo induce l’espressione della proteina del checkpoint immunitario PD-L1 e previene il rigetto immunitario per 50 giorni, dopo il trapianto in topi diabetici.
Le vie di segnalazione Wnt sono un gruppo di vie di trasduzione del segnale che iniziano con proteine che trasmettono segnali attraverso recettori posti sulla superficie della cellula. Queste vie di segnalazione utilizzano la comunicazione tra cellule vicine o la comunicazione all’interno della stessa cellula.
Questo nuovo studio contribuisce agli sforzi in corso per sviluppare terapie alternative per il trattamento del diabete, non basate sulla necessità di donatori, e che non richiedono la soppressione immunitaria.