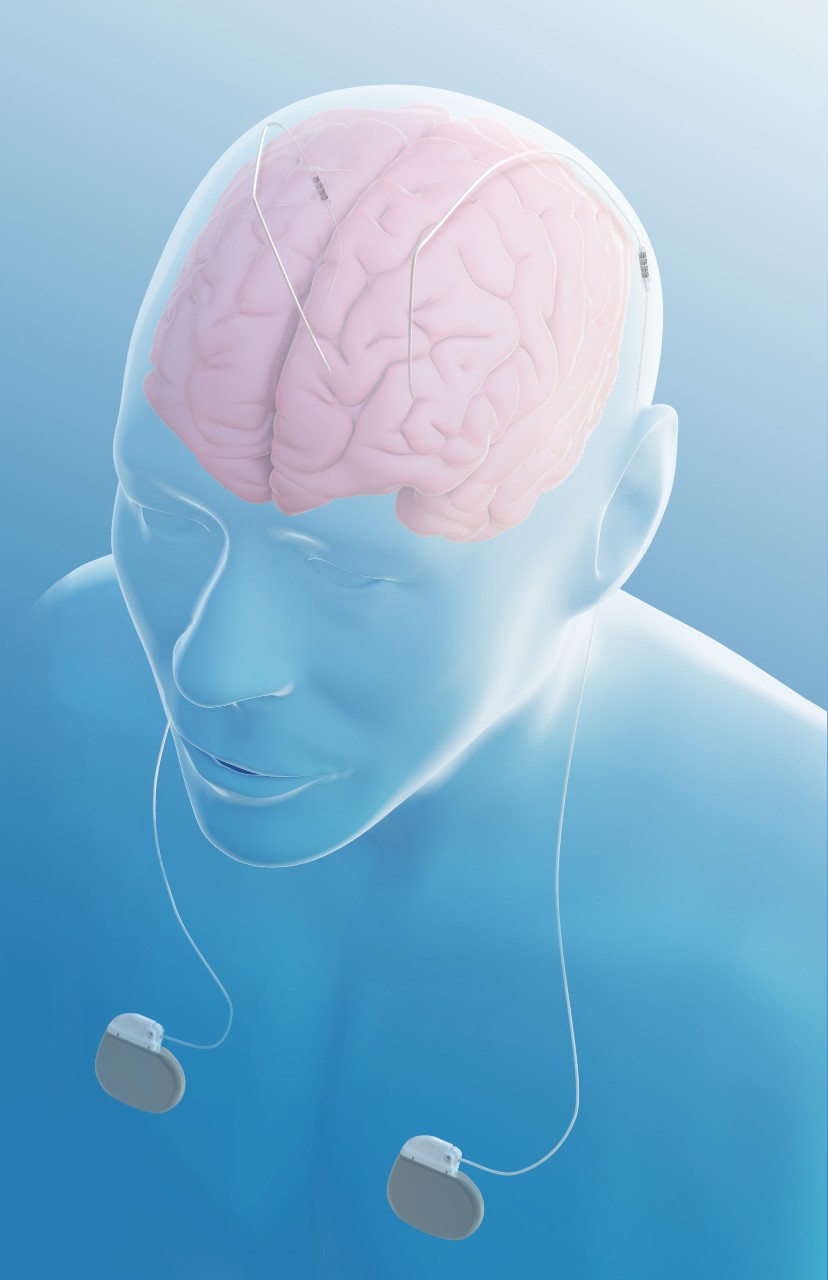
Il primo maggio scorso la Food and Drug Administration statunitense ha concesso l’approvazione pre-commerciale per la Deep Brain Stimulation (DBS) di Medtronic, da utilizzarsi come terapia aggiuntiva per ridurre la frequenza delle crisi comiziali ad esordio parziale, in individui di 18 anni o più che sono refrattari o resistenti a tre o più farmaci antiepilettici. La DBS per l’epilessia fornisce impulsi elettrici controllati a un bersaglio nel cervello chiamato nucleo anteriore del talamo, che fa parte di una rete coinvolta nello sviluppo delle crisi convulsive.
Secondo la Epilepsy Foundation, 3,4 milioni di individui negli Stati Uniti hanno l’epilessia. I farmaci antiepilettici sonno il trattamento principale per controllare le convulsioni, tuttavia, fino a un terzo delle persone con epilessia ha crisi comiziali che non rispondono con successo ai farmaci.
“Molti pazienti negli Stati Uniti con epilessia grave non sono in grado di controllare i loro attacchi con i farmaci attualmente disponibili e non sono candidati per la chirurgia potenzialmente curativa”, ha detto il dott. Robert Fisher, direttore dello Stanford Epilepsy Center, Stanford University, e sperimentatore principale dello studio SANTE. “L’epilessia refrattaria al trattamento con farmaci è un problema irrisolto e la DBS ora servirà come una nuova importante opzione di trattamento, anche per le persone con episodi ad origine poco localizzata o che coinvolgono regioni multiple”.
L’approvazione della FDA si basa sia sulla fase cieca che sui dati di follow-up a 7 anni raccolti nello studio clinico chiamato SANTE® (Stimulation of the Anterior Nucleus of the Thalamus in Epilepsy). Lo studio SANTE è stato uno studio clinico prospettico, randomizzato, in doppio cieco, per valutare l’uso della DBS nei pazienti con epilessia refrattaria, con crisi parziali, con o senza generalizzazione secondaria, che erano resistenti a tre o più farmaci antiepilettici. Lo studio ha raccolto dati da 110 pazienti che sono stati impiantati con un sistema Medtronic DBS in 17 centri situati negli Stati Uniti.
I risultati dello studio hanno evidenziato la riduzione media della frequenza di crisi totale dal basale del 40,4% contro il 14,5% per il gruppo placebo a 3 mesi e del 75% a 7 anni, con terapia in aperto. Venti soggetti (18%) hanno avuto almeno un periodo libero da crisi di 6 mesi tra l’impianto e l’anno 7, inclusi otto soggetti (7%) che erano liberi da crisi per i precedenti 2 anni. La gravità delle crisi convulsive e la qualità della vita hanno mostrato miglioramenti statisticamente significativi. Nessun declino cognitivo significativo o peggioramento dei punteggi di depressione sono stati osservati nel corso della fase in cieco o al 7 ° anno. A 7 anni sono stati rilevati punteggi migliori sia per le misure di funzioni esecutive, sia di attenzione.
“Siamo molto lieti di aver completato il processo di revisione per DBS per l’epilessia con la FDA, e siamo estremamente grati ai pazienti e ai loro team di trattamento per il loro impegno nello studio SANTE”, ha detto Mike Daly, vicepresidente e direttore generale del business Brain Modulation, che fa parte del gruppo Restorative Therapies di Medtronic. “Non vediamo l’ora di iniziare il lancio di questa terapia negli Stati Uniti nel corso di quest’anno”.